Медицинские изделия — это специальные устройства, которые используются в медицине для лечения, диагностики или профилактики заболеваний. Важным этапом в процессе производства и продажи медицинских изделий является их регистрация в соответствующих органах.
Регистрация медицинских изделий — это сложный процесс, требующий понимания многих юридических и технических аспектов. Неправильная регистрация может привести к штрафам, приостановлению производства или даже запрету на продажу изделий.
В данной статье мы предоставим вам пошаговое руководство, которое поможет правильно зарегистрировать медицинские изделия. Мы расскажем о необходимых документах, процедурах, требованиях и сроках, которые необходимо выполнить для успешной регистрации.
Первый шаг при регистрации медицинского изделия — определение его класса риска. Класс риска устанавливается в соответствии с международными стандартами IEC 60601 и ISO 14971 и зависит от предназначения и функционала изделия.
Категории медицинских изделий делятся на три класса: I, IIa, IIb и III. Класс риска устанавливается на основе биологического воздействия медицинского изделия на пациента, а также на основе его функциональности. Изделия класса I являются наименее опасными, а изделия класса III — наиболее опасными.
Для определения Регистрация медицинских изделий необходимо провести анализ его клинической эффективности и безопасности. Категория изделия зависит от степени воздействия на пациента и может изменяться в зависимости от его предназначения и функционала.
Категория медицинского изделия может быть определена на основе результатов клинических исследований и опыта использования. Все эти факторы должны учитываться при подаче заявки на регистрацию медицинского изделия.
Для регистрации медицинского изделия необходимо подготовить определенный пакет документов, который будет отправлен в соответствующий орган регистрации. Этот пакет должен содержать следующие документы:
- Заявление на регистрацию медицинского изделия;
- Паспорт медицинского изделия;
- Техническое описание медицинского изделия;
- Сертификаты качества и соответствия медицинского изделия;
- Результаты клинических испытаний медицинского изделия.
Заявление на регистрацию медицинского изделия должно содержать информацию о производителе изделия, его наименовании и характеристиках, а также о способе применения. Паспорт медицинского изделия должен содержать информацию о производителе, о его классификации по риску, об инструкции по применению.
Техническое описание медицинского изделия должно содержать информацию о его конструкции, технических характеристиках, а также о технологии производства. Сертификаты качества и соответствия медицинского изделия подтверждают его соответствие нормам безопасности и качества, установленным законодательством.
Результаты клинических испытаний медицинского изделия необходимы для подтверждения его эффективности и безопасности при использовании.
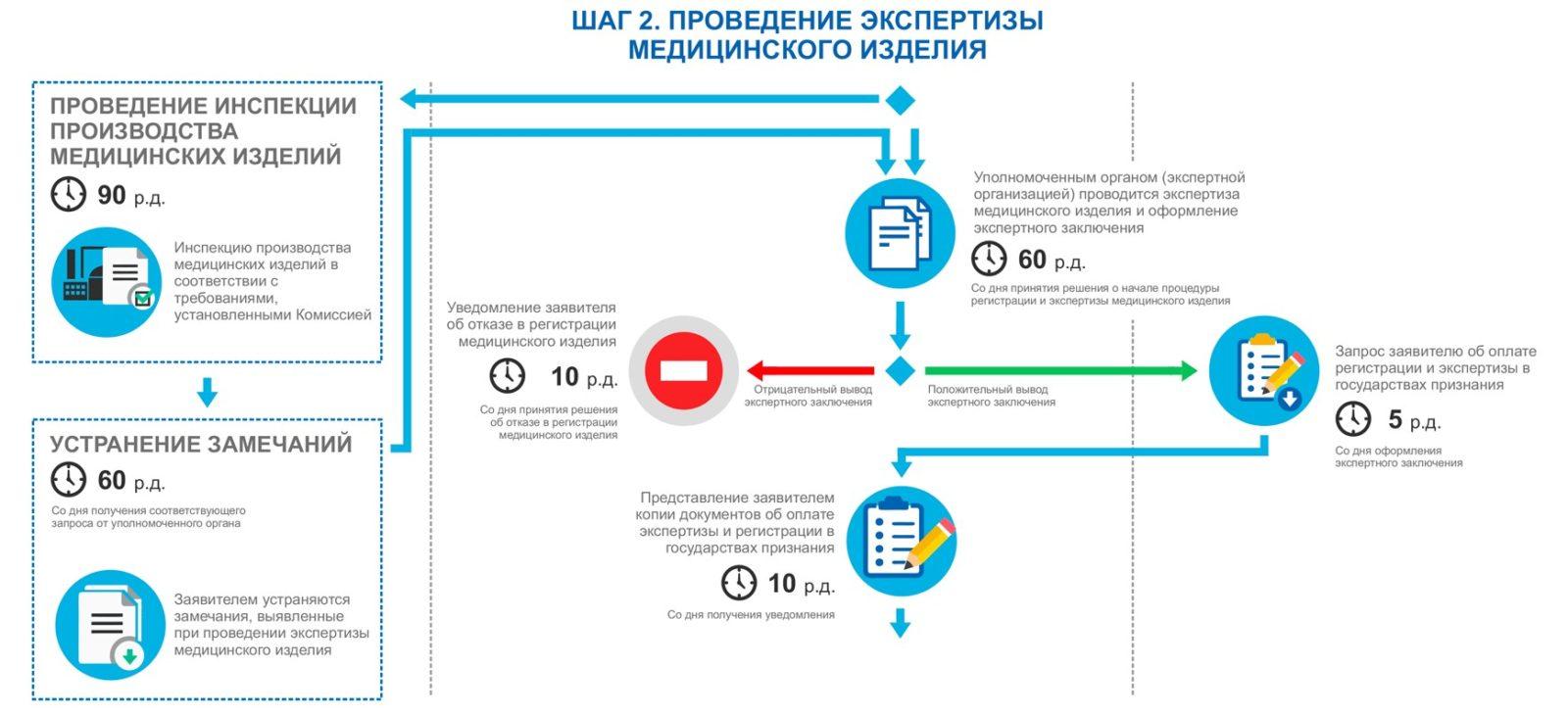
После проведения всех необходимых исследований и испытаний, а также подготовки пакета документации, необходимо подать заявление на регистрацию медицинского изделия в уполномоченный орган. Для этого необходимо следовать определенной процедуре и предоставить все необходимые документы.