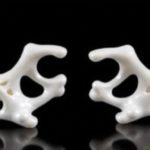
Разворот темы, который сейчас звучит как научная фантастика, на деле уже входит в клиническую реальность. Представьте себе персонализированную кость, идеально повторяющую форму дефекта, состыкованную с тканями организма и поддерживаемую на первых этапах за счёт специально созданного каркаса. Так сегодня выглядит направление 3D‑печати костной ткани в ортопедии. Это не просто новый гаджет на полке лаборатории — это подход, который может изменить результаты операций, сроки реабилитации и качество жизни пациентов. Мы поговорим о том, как устроены технологии, какие материалы задействуют, какие преимущества и риски несут, и какие шаги уже реально реализованы на клиническом уровне.
Содержание
- 1 Зачем нужна 3D‑печать костной ткани
- 2 Как работает биопечать костной ткани
- 3 Преимущества для пациентов
- 4 Таблица: сравнение подходов к костной ткани
- 5 Этапы внедрения в клинику
- 6 Проблемы и вызовы
- 7 Будущее и сценарии внедрения
- 8 Как выбрать направление для вашего центра или клиники
- 9 Что важно помнить прямо сейчас
- 10 Заключение
Зачем нужна 3D‑печать костной ткани
Когда речь заходит о сложных переломах, дефектах кости после травмы или удалении части кости по медицинским причинам, стандартные имплантаты порой не дают полного решения. Обычные части заменяют на готовые изделия, которые иногда не подходят по форме и размеру. Здесь на помощь приходит индивидуальная реконструкция: печать кости с учётом анатомии конкретного пациента.
Одной из главных идей является не просто заполнить пустоту, а воссоздать естественный микроскопический мир костной ткани. В ней есть канал Михаиловича — сосудистая сеть, клетки, матрица, сигнальные молекулы. Всё это должно работать вместе: поддерживать прочность, позволять кровоснабжению проникать в образовавшуюся структуру и со временем переходить к естественной регенерации. 3D‑печать костной ткани может дать и то, что ранее было доступно только в теоретических моделях — создание пористого каркаса, который обеспечивает прочность в нужной зоне и одновременно оставляет путь для формирования сосудов и новых клеток.
Технологии печати позволяют перейти от «готового имплантата» к «индивиуализированному имплантату», где форма, внутренние поры, биоматериалы и даже клеточные компоненты подбираются под конкретного пациента. Это снижает риск отторжения, ускоряет заживление и открывает дорогу к более точной химической настройке среды для костной регенерации.
Как работает биопечать костной ткани
Биопечать – это особый вид 3D‑печати, где создають не просто физическую форму, а живую модель ткани. В основе лежит сочетание биоматериалов (биоматериалы костной ткани), клеток, факторов роста и специальной среды для печати. Модульная система позволяет сначала напечатать структурную часть из каркаса, а затем заполнить её биоматериалами, богатым витаминно–модельным составом, чтобы клетки могли развиваться и интегрироваться в организм.
Ключевые элементы биопечати:
— Каркас или субстрат: пористый, чтобы в нём могли расти новые клетки и формироваться сосуды.
— Биоматериалы (биоинк): гели и матрицы, которые поддерживают клетки и передают им механические сигналы.
— Клеточные компоненты: стволовые клетки или предшественники костной ткани, которые способны к остеогенезу.
— Факторы роста: сигнальные молекулы, ускоряющие формирование костной ткани и кровоснабжение.
В практическом плане процесс выглядит так: сначала сканируют область дефекта, на основе данных создают трёхмерную модель. Затем подбирают материал и параметры печати. После этого печатают каркас и заполняют его биоматериалами с клетками. Далее идёт стадия инкубации и подготовки к имплантации: клетки должны пройти проверку безопасности, жизнеспособности и функциональности. В клинике имплантат вставляют в нужную зону, и начинается процесс интеграции с пациентом.
Материалы и биоматериалы
— Костные минеральные матрицы: гидроксиапатит (HA), трикалцийфосфат (TCP), их композитные варианты.
— Биоматериалы на основе коллагена, гиалуроновой кислоты и производных гидрогелей.
— Гидрогели на основе полимеров, которые поддерживают клетки и дают нужный микроклимат.
— Комбинированные системы: каркас из твердого материала с заполнением из биоактивного геля.
Главное — подобрать материал так, чтобы он сочетал прочность и биосовместимость, позволял клеткам расти и не вызывал токсических реакций. Важнейший момент — пористость каркаса: она должна быть достаточно открытой, чтобы сосуды могли расти внутрь, но при этом сохранять механическую прочность на нужном уровне.
Технологии печати
— Экструзионная биопечать: чаще всего используется для жидких или полужидких биоинк и для создания пористой структуры. Позволяет точно контролировать толщину слоёв и поры.
— Лазерно‑ассистированная печать: обеспечивает высокую точность и прочность за счёт локального расплавления или облучения материалов.
— Стереолитография и фотополимеризация: применяются с фотополимерными гелиями, где светом формируются твёрдые структуры в заданной форме.
— Комбинированные подходы: иногда в одну операцию объединяют несколько технологий, чтобы на выходе получить нужный микромир ткани и достаточную прочность.
Преимущества для пациентов
— Персонализация. Каркас и структура подгоняются под точный контур дефекта, что уменьшает риск несостыковок и осложнений.
— Быстрое восстановление. В некоторых случаях биоматериалы стимулируют регенерацию быстрее, чем традиционные методы.
— Улучшенная интеграция. Наличие пористости, поддерживающей кровоснабжение, способствует лучшему срастанию с окружающей костью.
— Меньше вторичных операций. Индивидуальные имплантаты подбираются под конкретную ситуацию, что может снизить потребность в повторной коррекции.
Таблица: сравнение подходов к костной ткани
| Метод | Материалы | Преимущества | Недостатки | Статус |
|---|---|---|---|---|
| Экструзионная биопечать | Гели с клетками, композиты на основе HA/TCP | Высокая точность слоя, возможность инкапсулировать клетки | Сложности со стабильностью био ink, требует контроляVi | Активно исследуется, клинических примеров немного |
| Лазерно‑ассистированная печать | Твердые материалы, композиты | Возможность высокой прочности и точности | Сложность в обработке живых клеток, ограничение материалов | Промышленный интерес, ограниченные клинические применения |
| Стереолитография | Фотополимеры, био Ink с фоточувствительными компонентами | Сложная геометрия, высокая детализация | Не все биоинки совместимы с фотополимеризацией | Развивающийся сектор, клинические этапы |
| Комбинированные решения | Каркас из твёрдого материала + биоинк | Баланс прочности и биоинтеграции | Сложная технология реализации | Управляемый рост практических кейсов |
- Персонализация под анатомию пациента на основе КТ и МРТ сканов.
- Контроль пористости и каналы сосудистого притока внутри каркаса.
- Интеграция клеточных компонентов для активной регенерации ткани.
- Регуляторная база и безопасность биоматериалов.
- Долгосрочная устойчивость имплантата в условиях физиологической нагрузки.
Этапы внедрения в клинику
— Диагностика и планирование. Точная трёхмерная модель зоны дефекта формируется по данным снимков пациента.
— Выбор подхода. В зависимости от локализации дефекта, нужной прочности и скорости восстановления выбирают материал и метод печати.
— Производство и тестирование. Печать каркаса, его заполнение биоink, тестирование на прочность и совместимость.
— Операция и послеоперационное ведение. Имплантация идет в рамках протоколов безопасности и регламентов клиники.
— Реабилитация. Включает динамический мониторинг регенерации, контроль за интеграцией и адаптацию физической нагрузки.
Проблемы и вызовы
— Механическая прочность vs биологическая активность. Каркас должен выдерживать нагрузку, но не мешать клеткам расти.
— Вариативность дефектов. Каждый случай уникален, и подходы не всегда применимы «как есть» к другой ситуации.
— Регуляторные вопросы. Одобрение новых материалов и процедур требует длительных испытаний и доказательств эффективности.
— Стоимость. Высокие затраты на оборудование, биоматериалы и компетентный персонал могут быть препятствием в рамках некоторых клиник.
— Этические аспекты. Использование клеток пациентов или донорских материалов требует строгого контроля и прозрачности.
Будущее и сценарии внедрения
— Интеграция с нанотехнологиями. Улучшение механических свойств за счёт наноструктур и направленной биостимуляции.
— Расширение спектра материалов. Разработка биоинк‑композитов, адаптирующихся под локальные условия нагрузки.
— Прецизионная регенерация. Импланты, которые «заселяются» клетками именно той ткани, где это нужно, и формируют сосудистую сеть по индивидуальному плану.
— Роль искусственного интеллекта. Помощь в планировании операций, прогнозировании прогресса регенерации и оптимизации биоматериалов под пациента.
— Этические и правовые рамки. Ведущие регуляторы всё чаще устанавливают единые стандарты качества и безопасности, что ускорит широкое внедрение.
Как выбрать направление для вашего центра или клиники
— Оценка доступной инфраструктуры. Наличие оборудования для сканирования, печати и лабораторной подготовки материалов.
— Квалификация команды. Требуется тесная работа хирургов, материаловедов, биологов и инженеров‑медиков.
— Клинические кейсы. Наличие реализованных проектов и публикаций в профильных журналах добавляет доверия.
— Финансовый план. Расчёт на долгосрочную окупаемость за счёт улучшенных исходов и расширения спектра услуг.
— Этический компас. Прозрачные процессы, информированное согласие пациентов и тщательная работа с материалами.
Что важно помнить прямо сейчас
— 3D‑печать костной ткани — мощная технология будущего, но она уже применяется сегодня в отдельных клинических случаях и демонстрирует устойчивый прогресс.
— Важна синхронизация нескольких дисциплин: материаловедения, биологии, инженерии и медицины. Успех зависит от слаженной команды и чётких протоколов.
— Ранняя клиническая адаптация требует аккуратного подхода: эксперименты и пилотные проекты должны сопровождаться строгой безопасностью и доказывать эффективность через данные.
Заключение
Итак, 3D‑печать костной ткани стоит на стыке инженерии и медицины, где идея перерастает в практику. Это путь к индивидуализированной ортопедии, где каждый имплантат подгоняется под форму и особенности пациента, обеспечивая более естественную регенерацию и более быструю реабилитацию. На этом пути перед нами стоят не только технические задачи, но и вопросы регуляторной поддержки, экономической доступности и этических норм. Но темп разработки впечатляет: новые биоматериалы, усовершенствованные методы печати и готовность клиник к внедрению уже сегодня создают реальный потенциал для смены парадигмы в лечении сложных костных дефектов. В ближайшие годы мы увидим не только отдельные случаи успешной биопечати, но и устойчивые практики, в которых персонализированные имплантаты станут нормой. Это будет не просто шаг вперёд, а новый горизонт в ортопедии, где технология служит человеку и помогает ему вернуться к привычной жизни без боли и ограничений.