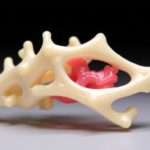
В мире медицины наступает эпоха, когда кость можно не просто лечить, а строить заново. 3D‑печать костной ткани превращает зачатки идей в реальные импланты и заготовки для хирургии, где каждый миллиметр индивидуален. Представьте себе стенку из множества слоев, каждый из которых создан под точные параметры конкретного пациента: форма, прочность, скорость интеграции с живыми тканями. Именно так работают современные исследования и клинические прототипы. И пока речь идет не только о красивых картинках в научных журналах, а о практических шагах к регенерации сложных костных дефектов после травм, опухолей или заболеваний.
Содержание
Что стоит за идеей 3D‑печати костной ткани
Каждый раз, когда мы говорим о 3D‑печати, вспоминаем слои: сначала создаются цифровые модели, потом принтер наносит тонкие витки материала, формируя пористую структуру, способную в eventual времени вести клеточную колонизацию и формирование собственной кости. Но здесь история не только о слоистой сборке. В ней лежит принцип биоинженерии: биоматериалы не просто заполняют форму будущего импланта, они взаимодействуют с клетками, направляя их на рост, деление и организацию сосудов, а значит — на долгую и устойчивую функциональность.
Ключевые преимущества 3D‑печати костной ткани перед традиционными методами замещения — индивидуализация и точность. Пациенту можно подобрать размер, геометрию и пористость, чтобы имплант максимально точно повторял естественную костную архитектуру. Это особенно важно при дефектах больших объемов, когда стандартные graft-материалы не дают нужной поддержки. В реальности мы видим переход от «готовых заготовок» к персонализированным решениям, где каждый имплант подгоняется под уникальные особенности пациента — от анатомии таза до длинной кости конечности.
| Характеристика | Традиционные методы | 3D‑печатная костная ткань |
|---|---|---|
| Индивидуализация | Стандартные формы, ограниченная адаптация | Полная адаптация под анатомию пациента |
| Пористость и структура | Немного вариативны | Контролируемые параметры пористости и межкристаллической архитектуры |
| Скорость производства | Долгий цикл подготовки | Быстрая конвейерная настройка под дефект |
| Коммуникация с клетками | В большинстве случаев ограниченная | Драйверы роста и биоматериалы стимулируют остеогенез |
Однако перевести идею в практику — задача сложная. Проблемы разделяются на инженерные и клинические. Инженерные включают в себя создание материалов, которые сочетают прочность и биосовместимость, а также обеспечение сосудистой иннервации будущей кости. Клинические вызовы — это проверка долговременной безопасности, совместимости с тканями организма и регуляторные вопросы, которые сопровождают любую новую медицинскую технологию.
Сейчас наш разговор не о фантазиях будущего, а о реальном прогрессе, который уже помогает врачам. Мы видим, как растет качество цифровых моделей, улучшаются прагматичные биозаполнители и разворачивается цикл клинических испытаний. Ключ к успеху — грамотное сочетание материалов, биоинженерного дизайна и биологической подготовки пациента к вмешательству.
Материалы и методы 3D‑печати костной ткани
Сектор материалов для костной регенерации активно развивает три направления: биополимерные матрицы, керамические фазы и композитные системы. Каждый из подходов имеет свои сильные стороны и ограничения, и современные решения чаще всего строятся на их сочетании.
- Гидроксиапатит и фосфат кальция — основа костной минерализации. Эти материалы хорошо поддерживают приток кальция и минеральную часть зрелой кости, но сами по себе не всегда обладают достаточной прочностью.
- Биополимеры, например PLA, PLGA, полиуретаны — управляемая деградация во времени. Они служат каркасом и средой для клеток, постепенно исчезая по мере формирования собственной ткани.
- Композитные подходы — сочетание керамики и полимера дают баланс между прочностью и биосовместимостью. Такие материалы чаще всего применяются в больших дефектах, требующих долгосрочной поддержки.
- Гидрогели и биоинклеры — биологически активные среды, которые могут включать ростовые факторы и клетки. Они особенно перспективны в биопринтинге вместе с клетками.
Технологии печати делятся на несколько классов. В большинстве лабораторий работают с методами, которые позволяют создавать пористые структуры и точно размещать биоматериалы в требуемой геометрии. Среди популярных подходов — струйная печать, лазерная селективная сплавка, экструзия биочернил и сферы гель‑матриц, которые нуждаются в дополнительной стабилизации. Каждый метод имеет свои требования к объему, точности и совместимости с живыми клетками. В клинике, где речь идет об имплантах, особенно важна стерильность и надежность изготовления.
Биоматериалы и биоинженерные принципы
Чтобы кость стала функциональной, важно не только построить каркас, но и активировать регенеративные процессы в организме пациента. Применяются как внешние материалы, так и внутрикостные биоинжекции. В одном проекте могут сочетаться частично переработанные керамические компоненты и полимерная матрица, наполненная остеогенными клетками или факторами роста. Такой подход помогает организовать образование сосудов и минерализацию ткани.
Применение сосудистой инфраструктуры
Без квалифицированной сосудистой сети новая кость не сможет правильно питаться и расти. Поэтому в исследованиях особенное место занимает микроканальная архитектура каркасов и внедрение факторов, способствующих ангиогенезу. Иногда в принтинг включают клетки эндотелия или подкожные клетки стромы, чтобы ускорить формирование кровообращения в заготовке. Когда речь заходит о клинике, эта часть проекта становится критической в плане долговременного функционирования импланта.
Клинические приложения 3D‑печатной костной ткани
На практике мы видим несколько направлений, где 3D‑печать костной ткани уже приносит ощутимую пользу. В травматологии, онкологии и реконструктивной хирургии такие методы помогают воспроизводить сложные дефекты, улучшать приживаемость имплантов и ускорять реабилитацию пациентов. Пока речь о широком внедрении продолжается в рамках клинических испытаний, но темпы развития впечатляют.
Травматология и реконструкция
Дефекты длинных костей, тазовых костей, черепно-лицевой области — это сферы, где персонализированные каркасы способны существенно снизить риск повторного дефекта и улучшить функциональные результаты. В таких случаях 3D‑печатная кость может служить как временный каркас до заживления собственной ткани, так и как постоянный элемент, который участвует в биологической интеграции на протяжении многих лет.
Замещение дефектов и регенеративная хирургия
При крупных резекциях злокачественных опухолей или врожденных дефектах порой требуется заполнить объем тканей, которые невозможно восстановить естественным путем. Здесь 3D‑печатные структуры предоставляют точную геометрию и чёткую переработку материалов под конкретного пациента. В некоторых случаях применяют биопринтинг с клетками, чтобы стимулировать локальный рост кости прямо в области дефекта.
Образование и планирование операций
Помимо непосредственной замены ткани, 3D‑печать позволяет создавать точные модельные заготовки для планирования сложных вмешательств. Хирурги получают возможность протестировать посадку импланта, оценить риск осложнений и выбрать наилучший маршрут операции еще до начала разрезов. Это снижает время операции и улучшает предсказуемость исхода.
- Преимущества
- Персонализация под анатомию пациента
- Улучшенная интеграция тканей
- Снижение времени операции в некоторых случаях
| Фактор | Риски | Контроль и mitigations |
|---|---|---|
| Гиперстатичность импланта | Неправильная адаптация может привести к микродефрагирования | Точная цифровая модель и прецизионная сборка |
| Долгосрочная биосовместимость | Риски хронического воспаления | Использование сертифицированных материалов и мониторинг |
| Сосудистая иннервация | Недостаток кровоснабжения в центре структуры | Инженерия пористости и ангиогенез через факторы роста |
Несмотря на сложности, клинические данные постепенно устойчиво показывают преимущества костной печати по сравнению с традиционными подходами в узких случаях. В руководствах производителей материалов и клиник все чаще встречаются параметры качества, которые учитывают не только механическую прочность, но и биологическую активность. Это важный шаг к тому, чтобы 3D‑печать костной ткани стала частью повседневной практики, а не редким экспериментом.
Этические, регуляторные и практические аспекты
Любая новая медицинская технология должна проходить строгий контроль. Здесь важны этические принципы, прозрачность клинических данных и четкие стандарты качества. Пациентам необходимо объяснять не только преимущества, но и ограничения, риски и возможное отсутствие долгосрочных данных. В регуляторном поле происходят адаптации под быстро развивающийся сегмент: стандарты безопасности, критерии одобрения и надлежащая подготовка персонала. Всё это направлено на то, чтобы инновации приносили реальную пользу без угрозы для здоровья.
Практически это означает тесное сотрудничество хирургов, биоинженеров, материаловедов и регуляторных специалистов. Только общая работа поможет превратить лабораторные прототипы в безопасные и эффективные решения для пациентов. Также важно развитие образовательных программ: врачи и технический персонал должны понимать принципы печати, характеристики материалов и принципы контроля качества, чтобы в ближайшие годы расширять круг клинических ситуаций, где возможно применение 3D‑печати костной ткани.
Будущее 3D‑печати костной ткани: что ждать
Горизонт ближайших лет обещает объединение всех элементов в целостную экосистему лекарств и имплантов. Мы увидим более точные биоматериалы с усиленной биоактивностью, новые биопринтинговые «чернила», которые будут включать клетки, медиаторы роста и даже микроорганизмы, помогающие заживлению. Важной станет оптимизация процессов в реальном времени: цифровой мониторинг, адаптация параметров печати под динамику регенерации, интеграция с радиологией и биоинженерной тактикой. Все это приведет к тому, что качество жизни пациентов после операций по реконструкции костей заметно вырастет, а периоды восстановления станут короче.
Но вместе с возможностями растут и требования к ответственности. Клиникам и производителям предстоит обеспечить повторяемость и безопасность на каждом этапе: от проектирования до установки импланта и контроля послеоперационного процесса. Этическая готовность общества к новым подходам в лечении травм и дефектов костей станет не менее важной, чем сами технологии. В этом контексте открытое обсуждение, пролонгированные исследования и внимательное отношение к каждому пациенту будут основой доверия и устойчивого прогресса.
Заключение
3D‑печать костной ткани — это больше, чем инновационная технология. Это мост между детальной инженерией и живой биологией, который помогает воспроизводить сложные структуры и поддерживать естественные процессы заживления. Мы на пороге практического внедрения персонализированных имплантов, которые учитывают форму тела, место дефекта и скорость регенерации. Реальная клиника уже пользуется заготовками и иногда готовыми каркасами, а коррекции под конкретного пациента становятся нормой.
Темпы развития впечатляют, но главное — ясная дорожная карта от идеи до безопасной практики. Уже сегодня мы видим, как материалы становятся прочнее и одновременно более биосовместимыми, как каркасы учатся «дышать» сосудистой сетью, и как врачи учатся работать с этими новшествами, не забывая о пациентах. Будущее, в котором каждый дефект кости можно восполнить с учетом индивидуальных потребностей, приближается. И когда все элементы сойдутся воедино — биоматериалы,打印 технологии, клинические протоколы и регуляторные рамки — мы увидим новый стандарт реконструктивной медицины, где восстановление становится точной наукой и искусством одновременно.